Research Article
Auditory brainstem
responses in children treated with cisplatin
Mahsa
Bakhit1, Akram Pourbakht1, Masoumeh Rouzbahani1,
Shahla Ansari2, Mohammad Kamali3
1- Department of Audiology,
Faculty of Rehabilitation, Tehran University of Medical Sciences, Iran
2- Clinic of Hematology and
Oncology of Children, Ali Asghar Hospital, Tehran University of Medical
Sciences, Iran
3- Department of Rehabilitation
Management, Faculty of Rehabilitation, Tehran University of Medical Sciences,
Iran
Received:
17 May 2011, accepted: 6 November 2011
Abstract
Background and Aim: In view of
improvement in therapeutic outcome of cancer treatment in children resulting in
increased survival rates and the importance of hearing in speech and language
development, this research project was intended to assess the effects of cisplatin
group on hearing ability in children aged 6 months to 12 years.
Methods: In this cross-sectional
study, hearing of 10 children on cisplatin group medication for cancer who met
the inclusion criteria was examined by recording auditory brainstem responses
(ABR) using the three stimulants of click and 4 and 8 kHz tone bursts. All
children were examined twice: before drug administration and within 72 hours
after receiving the last dose. Then the results were compared with each other.
Results: There was a
significant difference between hearing thresholds before and after drug
administration (p<0.05). Right and left ear threshold comparison revealed no
significant difference.
Conclusion: Ototoxic effects
of cisplatin group were confirmed in this study. Insignificant difference
observed in comparing right and left ear hearing thresholds could be due to
small sample size. auditory brainstem responses test especially with frequency
specificity proved to be a useful method in assessing cisplatin ototoxicity.
Keywords: Cisplatin, carboplatin,
ototoxicity, children, auditory brainstem responses
مقالۀ
پژوهشی
بررسی
پاسخهای شنوایی ساقۀ مغز در کودکان تحت درمان با
خانوادۀ دارویی سیسپلاتین
مهسا بخیت1، اکرم پوربخت1،
معصومه روزبهانی1،
شهلا انصاری2،
محمد کمالی3
1ـ گروه
شنواییشناسی، دانشکده توانبخشی، دانشگاه علوم
پزشکی تهران، ایران
2ـ بخش هماتولوژی و انکولوژی کودکان
بیمارستان حضرت علیاصغر(ع)، دانشگاه علوم پزشکی تهران،
ایران
3ـ گروه مدیریت
توانبخشی، دانشکده توانبخشی،
دانشگاه علوم پزشکی تهران، ایران
چکیده
زمینه و هدف: نظر به افزایش تعداد
کودکانی که از بیماری سرطان جان سالم به در میبرند و با
توجه به اهمیت شنوايي در رشد گفتار و زبان، این پژوهش اقدام به
بررسی تأثیر خانوادۀ دارویی سیسپلاتین
بر شنوایی کودکان شش ماه تا دوازده سال مبتلا به سرطان نمود.
روش بررسی: در این پژوهش مقطعی، 10 کودک
تحت درمان با گروه دارویی سیسپلاتین که شرایط ورود
به طرح را داشتند، توسط آزمون پاسخهای شنوایی ساقۀ مغز
با سه محرك کلیک، تنبرست 4000 و 8000 هرتز و
طی دو مرحله، یکبار قبل از دریافت داروی
شیمیدرمانی و یکبار 72 ساعت پس از دريافت آخرين دوز دارو،
مورد بررسي قرار گرفتند. سپس نتایج با هم مقایسه شد.
یافتهها: تفاوت
آستانههای شنوایی قبل و بعد از دریافت دارو برای
کلیک، تنبرست 4000 و 8000 هرتز معنیدار بود(05/0(p<. آستانههای گوش چپ و
راست تفاوت معنیداری را نشان نداد.
نتیجهگیری: در اين مطالعه تأثیر نامطلوب
خانوادۀ دارویی سیسپلاتین بر ایجاد افت
شنوایی تأیید شد. تفاوت تغييرات آستانه گوش چپ و راست معنیدار
نبود که میتواند به واسطۀ تعداد کم نمونهها باشد. بهطور كلي نتايج
اين مطالعه تأييد کرد كه پاسخهای شنوایی ساقه مغز بهویژه
با استفاده از ویژگی فرکانسي، ابزاری ارزشمند در بررسی
مسموميت گوشي ناشي از خانوادۀ دارويي سيسپلاتين باشد.
واژگان کلیدی: سیسپلاتین، کربوپلاتین، مسمومیت گوش،
کودکان، پاسخهای
شنوایی ساقۀ مغز
(دریافت مقاله: 27/2/90،
پذیرش: 15/8/90)
مقدمه
سیسـکلرودیآمینوپلاتین
(سیسپلاتین) و پاراپلاتین (کربوپلاتین) از ترکیبات
پلاتینوم بوده و جزء خانوادۀ دارويي سيسپلاتين محسوب ميشوند.
این داروها بهطور گسترده برای درمان سرطانهای سر و گردن،
استخوان، کبد، مثانه، تخمدان، بیضه، ششها، نوروبلاستوما و برخی
تومورهای سیستم عصبی مرکزی به کار میروند(1). همچنین
عوارض جانبی متعددی دارند که عمدهترین آنها تهوع، استفراغ،
درگیری اعصاب محیطی، آسیب به کلیه و
مسمومیت گوش (ototoxicity) است(2). اتوتوکسیک بودن سیسپلاتین در سال 1972
شناسایی و گزارش شد و در بین ترکیبات پلاتینوم بهعنوان
مسمومیتزاترین دارو معرفی شد(1). مکانیسم اثر آن به این
صورت است که سیسپلاتین به اتم N7
اسید نوکلئیکپورین در مولکول دئوکسیریبونوکلئیک
اسید (Deoxyribonucleic acid: DNA)
متصل شده و این اتصال مانع همانندسازی و رونویسی مطلوب DNA
و در نهایت تخریب سلولی میشود. البته ممکن است به مولکولهای
غیر DNA مانند پروتئینها نیز متصل شده و باعث تولید
رادیکالهای آزاد و مهار آنتیاکسیدانهای
داخلی شود. بنابراين براساس تحقیقات Rybak
و
همکاران (2007) در مسمومیت گوشی ناشی از سیسپلاتین
تخریب ناشی از تولید رادیکالهای آزاد مطرح است(3).
در مطالعۀ دیگری که توسط Truong و همکاران (2007) صورت
گرفت، نتایج حاکی از این بود که سلولهای حاشیهای،
نوار عروقی و سلولهای مویی خارجی بهدلیل
فعالیت سلولی و تغذیۀ عروقی بالا، نسبت به اثرات مسمومیت
گوشی مستعدترند و بیشتر آسیب میبینند(4).
مطالعۀ Toral-Martiñón و همکاران (2003) نشان داد که کودکان نسبت به مسمومیت گوشی
این دارو، بهًویژه دوزهای بالای آن (400-200
میلی گرم) حساسترند و شیوع افت شنوایی ناشی
از سیسپلاتین در کودکان، 50 تا 88 درصد گزارش شده است(5). نتایج حاصل از مطالعۀ Fausti و همکاران در سال 2007 نشان داد که علائم مسمومیت
گوشی ممکن است بعد از ارائۀ یک دوز دارو مشاهده شوند و یا
برای روزها و ماهها تأخیر داشته باشند. علائم معمولاً پیشرونده
و دائمی هستند و خطر افت شنوایی معمولاً مرتبط با دوز
تجمعی دارو است(6). با در نظر گرفتن حال
عمومی کودکان سرطانی، انجام آزمونهای رفتاری دشوار است و
امروزه برای پایش وضعیت شنوایی این کودکان بهدنبال
آزمونهای عینی (آبجکتیوی) هستند. گسیلهای
صوتی گوش
(Otoacoustic Emissions: OAE)
و پاسخهای شنوایی ساقۀ مغز (Auditory
Brainstem Responses: ABR) نمونههایی
از این آزمونهای عینی هستند. آزمون OAE هرچند نیازمند پاسخهای رفتاری کودک نیست، اما
وجود اوتیت میانی و گریۀ احتمالی کودک
میتواند ثبت پاسخ را با اشکال رو به رو سازد(7).
یکی
از پتانسیلهای برانگیختۀ شنوایی ABR است كه مستقل از هوشیاری فرد بوده و در تخمین
حساسیت شنوایی و نیز در ارزیابیهای
اوتونورولوژیک با هدف تشخیص ضایعات عصب شنوایی و
مسیرهای شنوایی در ساقۀ مغز اعتبار و کاربرد
بالایی دارد(8و9).
در
سنین کودکی، حفظ شنوایی اهمیتی چند برابر
مییابد، چرا که کودکان در حال دریافت اطلاعات
شنوایی و یادگیری زبان و گفتار بوده و افت
شنوایی در آنان، بهخصوص در فركانسهاي بالا، میتواند با از
دست رفتن واجهای صامت و به عبارتی واجهای سایشی منجر
به تأخیر در رشد گفتار و زبان و نیز عقبماندگیهای
تحصیلی و اختلال در تواناییهای ارتباطی کودک
شود(10و11). با توجه به اين
که با پیشرفت علوم پزشکی، تعداد بیشتری از کودکان از
سرطانهای دوران کودکی جان سالم به در میبرند، اهمیت
حفاظت شنوایی و پیشگیری از اختلالات
شنوایی صد چندان میگردد(12). با این وجود، متأسفانه به
ندرت پایش شنوایی کودکان حین مصرف اين داروها بهطور جدي
اجرا میشود. بنابر آنچه گفته شد و نظر به عدم پیشینۀ انجام
چنین مطالعهای در ایران، در این پژوهش اثراتِ زودهنگام
مصرف خانوادۀ دارویی سیسپلاتین بر
شنوایی کودکان مبتلا به سرطان با استفاده از آزمونABR بررسی شد.
روش بررسی
پژوهش
حاضر از نوع بررسي مقطعي بوده و در کلینیک شنواییشناسی
دانشکده توانبخشی دانشگاه علوم پزشکی تهران و با همکاری
بیمارستان کودکان حضرت علیاصغر (ع) انجام شد. روش نمونهگیری
بهصورت غیرتصادفی تدریجی بود. جامعۀ مورد مطالعه،
کودکان شش ماه تا 12سالۀ تحت درمان با گروه دارویی سیسپلاتین
بودند که تحت نظارت پزشک متخصص سرطانشناسی، در فاصلۀ زمانی
زمستان 1388 تا تابستان 1389 از بخش شیمیدرمانی
بیمارستان کودکان حضرت علیاصغر (ع) ارجاع داده میشدند. از
تعداد 10 بیمار شرکتکننده در این پژوهش، شش نفر مبتلا به
رتینوبلاستوما، سه نفر مبتلا به نوروبلاستوما و یک نفر مبتلا به تومور
ژرم سل بودند. از این تعداد، چهار نفر کربوپلاتین و شش نفر سیسپلاتین
دریافت میکردند. معيارهاي ورود کودکان به مطالعه شامل مصرف سیسپلاتین
یا کربوپلاتین بهعنوان داروی شیمیدرمانی از
شروع دورۀ درمان، عدم مصرف دیگر داروهای اتوتوکسیک بهطور
همزمان، نداشتن اختلالات و نارساییهای کلیوی،
پاتولوژی گوش میانی، عدم سابقۀ قرار گرفتن طولانی
مدت در معرض نویز بلند، عدم سابقۀ پرتودرمانی در سر و گردن قبل
یا همزمان با دریافت دارو و مساعد بودن حال عمومی کودک بود.
میانگین
دوز داروی دریافتی برای سیسپلاتین 67/113
میلی گرم بر هر متر مربع سطح بدن با انحراف معیار 791/14 و
برای داروی کربوپلاتین 00/210 میلی گرم بر هر متر
مربع سطح بدن با انحراف معیار 452/53 بود. لازم به ذکر است که رژیمهای
شیمیدرمانی معمولاً به شکل دورهای تجویز میشوند.
رژیم درمانی در رابطه با داروی سیسپلاتین،
میزان 20 میلی گرم بر متر مربع سطح بدن در هر روز بهصورت
تزریق وریدی برای مدت پنج روز یا 50-70 میلی
گرم بر متر مربع سطح بدن بهعنوان یک تک دوز و هر سه هفته
یکبار بوده و این مقدار برای داروی کربوپلاتین 360
میلی گرم بر متر مربع سطح بدن بهصورت تزریق وریدی
و هر چهار هفته یکبار است(13). بیمار طی چندین دوره و در فواصل سه
یا چهار هفتهای برای دریافت داروی خود به
بیمارستان مراجعه میکند. از تعداد 10 کودک شرکتکننده در این
پژوهش، هشت کودک در هنگام مراجعۀ اولیه به کلینیک
شنواییشناسی در ابتدای دریافت دورۀ دوم
شیمیدرمانی و دو کودک در ابتدای دریافت دورۀ
اول شیمیدرمانی خود بودند و سطح شنوایی آنها
طی دو مرحله، یکبار قبل از دریافت دارو و یکبار پس از
آن (حداکثر به فاصلۀ 72 ساعت پس از اتمام دریافت دارو) با استفاده از ABR
با محرکهای کلیک و تنبرست 4000 و 8000 هرتز مورد
ارزیابی قرار گرفت.
آزمون
دراتاقک ضد صدا و با استفاده از دستگاه ERA 2250
ساخت شرکت Madsen دانمارک و گوشی ER3A انجام میشد.
بیمار در وضعیت راحت قرار میگرفت، امواج تولید شده از
ساقۀ مغز توسط الکترودهای مستقر بر پیشانی (الکترود
مثبت)، بر ماستوئید گوش
آزمایشی (الکترود منفی) و بر ماستوئید گوش
غیرآزمایشی (الکترود مشترک) ثبت شده و آستانۀ موج V
در امواج مذکور مورد بررسی قرار میگرفت. برای ثبت ABR،
20 محرک در هر ثانیه با قطبیت متناوب و دیرش 1/0 ثانیه
برای کلیک تنظیم میشد و برای محرک تنبرست از
الگوی Blackman استفاده میشد(9). زمان تحلیل آزمون 20
میلی ثانیه و از پالایشگر 150 تا 2500 هرتز بود. تعداد
2000 محرک در هر بار ثبت امواج به کار میرفت. آزمون از سطح شدتی 100 دسیبل SPLشروع میشد و در
صورتی که در این سطح پاسخی مشاهده نمیشد، سطح شدت در گامهای
10 دسیبلی تا مشخص شدن موج V
افزایش مییافت، و چنانچه در سطح 100 دسیبل
SPLموج V
مشاهده میشد، سطح شدت بهتدریج تا کمترین حدی که موجV قابل ردیابی بود کاهش داده میشد و سطح شدت
مذکور بهعنوان آستانۀ موج V در آن فرکانس خاص تعیین میشد. پس از انجام
آزمون در هر دو مرحله، نتایج با استفاده از نرمافزارSPSS نسخۀ شمارۀ 17 بررسی شد. به این منظور،
ابتدا با استفاده از آزمون آماری کولموگروفـاسمیرنوف وجود
توزیع هنجار در دادهها بررسی شد که با توجه به تأیید
وجود توزیع هنجار، آزمونهای آماری t زوج و tمستقل بهترتیب برای
بررسی معنیدار بودنِ تغییرات آستانه و تفاوت بین
دو گوش و قبل و بعد از دریافت دارو به کار رفت.
از
تمامی والدین رضایتنامۀ کتبی برای مشارکت
فرزندشان در پژوهش دریافت شد و والدين در تداوم یا قطع همکاری
با پژوهش اختیار تام داشتند. شرایط حاد بیماران شرکتکننده در
طرح و معیارهای ورود و خروج و نیز عدم امکان اجرای آزمونها
در محیط بیمارستان و عدم همکاری برخی از بیماران در
مراجعه به کلینیک شنواییشناسی، از جمله
مسائلی بود که باعث کاهش تعداد نمونهها شد. این پژوهش، منطبق بر
معاهدۀ هلسینکی و توکیو بوده و مورد تأیید
کمیتۀ اخلاق پزشکی دانشگاه علوم پزشکی تهران قرار گرفت.
یافتهها
بهمنظور
بررسی اثرات زودهنگام خانوادۀ دارویی سیسپلاتین،
نتایج حاصل از آزمون ABR قبل و بعد از دریافت دارو با یکدیگر
مقایسه شد. در این یافتهها، میانگین آستانههای
موج Vبا استفاده از محرک کلیک
قبل از دریافت دارو، در گوش راست 50/40 با انحراف معیار 66/10 دسیبل SPLبوده و این
مقدار پس از دریافت دارو ( حداکثر به فاصله سه روز از خاتمۀ
دریافت دارو) به 50/52 با انحراف معیار 14/15 دسیبل SPL
رسید. این
مقادیر برای گوش چپ بهترتیب 45 با انحراف معیار 43/9 دسیبل SPL و 50/56 با انحراف معیار 55/13 دسیبل SPL بود.
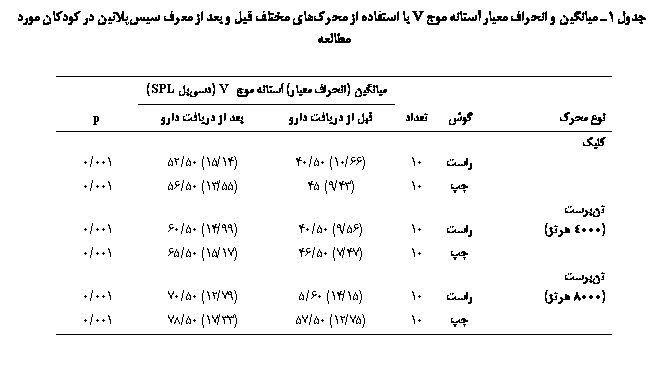 میانگین
آستانههای موج V برای محرک تنبرست 4000 هرتز قبل از دریافت دارو، در
گوش راست 50/40 با انحراف معیار 56/9 دسیبل SPL بود که پس از دریافت دارو، به 50/60 با انحراف معیار 99/14
دسیبل SPL رسید. مقادیر مذکور برای گوش
چپ، بهترتیب 50/46 و 50/65 با انحراف معیار 47/7 و 17/15 دسیبل
SPL بود. میانگین آستانههای موج Vبرای محرک تنبرست 8000
هرتز قبل از دریافت دارو، در گوش راست 50/56 با انحراف معیار 15/14
دسیبل SPL و پس از دریافت دارو 50/70 با انحراف معیار 791/12 دسیبل SPL بود. مقادیر مذکور برای گوش چپ بهترتیب 50/57 و
50/78 با انحراف معیار 75/12 و 33/17 دسیبل SPL بود. میانگین تغییرات آستانۀ موجV برای محرکهای کلیک، تنبرست 4000 هرتز و 8000 هرتز، بهترتیب
75/11 دسیبل SPL با انحراف معیار
635/9، 5/19 دسیبل SPL با انحراف معیار 659/13 و 5/17
دسیبل SPL با انحراف معیار 722/12 بهدست آمد. تغییرات
آستانه، قبل و بعد از دریافت دارو برای هر سه محرک کلیک و محرک
تنبرست 4000 و 8000 هرتز معنیدار بود(001/0p<) که در جدول 1 نشان داده شده است.
میانگین
آستانههای موج V برای محرک تنبرست 4000 هرتز قبل از دریافت دارو، در
گوش راست 50/40 با انحراف معیار 56/9 دسیبل SPL بود که پس از دریافت دارو، به 50/60 با انحراف معیار 99/14
دسیبل SPL رسید. مقادیر مذکور برای گوش
چپ، بهترتیب 50/46 و 50/65 با انحراف معیار 47/7 و 17/15 دسیبل
SPL بود. میانگین آستانههای موج Vبرای محرک تنبرست 8000
هرتز قبل از دریافت دارو، در گوش راست 50/56 با انحراف معیار 15/14
دسیبل SPL و پس از دریافت دارو 50/70 با انحراف معیار 791/12 دسیبل SPL بود. مقادیر مذکور برای گوش چپ بهترتیب 50/57 و
50/78 با انحراف معیار 75/12 و 33/17 دسیبل SPL بود. میانگین تغییرات آستانۀ موجV برای محرکهای کلیک، تنبرست 4000 هرتز و 8000 هرتز، بهترتیب
75/11 دسیبل SPL با انحراف معیار
635/9، 5/19 دسیبل SPL با انحراف معیار 659/13 و 5/17
دسیبل SPL با انحراف معیار 722/12 بهدست آمد. تغییرات
آستانه، قبل و بعد از دریافت دارو برای هر سه محرک کلیک و محرک
تنبرست 4000 و 8000 هرتز معنیدار بود(001/0p<) که در جدول 1 نشان داده شده است.
مقایسۀ
میزان تغییر آستانۀ موج V
در گوش چپ و راست با استفاده از آزمونt مستقل بیانگر
عدم تفاوت معنیدار بین دو گوش در محرکهای کلیک و تنبرست
4000 و 8000 هرتز بود(05/0<p).
مقدار شاخص p بهدست آمده برای تفاوت بین دو گوش با محرک
کلیک 54/0،
برای محرک تنبرست 4000 هرتز، 96/0 و
با محرک کلیک 8000 هرتز، 68/0 بود.
بحث
براساس
نتایج حاصل از این پژوهش، تأثیرات نامطلوب خانوادۀ
دارویی سیسپلاتین بر شنوایی و ایجاد
افت شنوایی تأیید شد و این مسئله اهمیت
پایش دقیق شنوایی افراد تحت درمان با این خانواده
دارویی بهویژه کودکان را نشان میدهد. شیوۀ
اثرگذاری این داروها عمدتاً بر فرکانسهای بالای
شنوایی بود که در اکثر بیماران پژوهش حاضر نیز مشاهده شد.
برخی بیماران در ABR با
محرک کلیک از شنوایی نسبتاً مطلوبی برخوردار بودند، در
حالی که نتایج حاصل از ABR با محرک تنبرست 8000 هرتز افت شنوایی را نشان
میداد. البته این مسئله به معنای نادیده گرفتن
سایر فرکانسهای شنوایی نیست. یادآوری
میشود که تغییرات آستانهای مشاهده شده در این
پژوهش، بیانگر تأثیرات زودهنگام این داروها بوده و نباید
از اثرات تأخیری احتمالی غافل بود. همانگونه که پیشتر
مطرح شد، پژوهش حاضر تأثیرات دریافت دارو را بهصورت زودهنگام و
حداکثر طی 72 ساعت پس از دریافت دارو بررسی کرده است و از
این رو احتمال افزایش افت شنوایی بیماران با گذر
زمان را منتفی نمیداند.
نتايج پژوهش حاضر، بيانگر تغييرات قابل
ملاحظه در آستانههاي شنوایی در فركانسهای بالا بود. البته از جمله محدودیتهاي اصلی
این تحقیق عدم
دسترسی به ABRبا محرك تنبرست
در فرکانسهاي بالاتر
از 8000 هرتز بود. با این وجود، تغییرات
مشاهده شده در نتایج آزمون تنبرست با فرکانس 8000 هرتز معنیدار بوده و در برخی
از بیماران عليرغم وجود نتايج طبيعي در محرك كليك، نتایج با تنبرست 8000
هرتز، حاکی از وجود افت شنوایی بود. از این رو، استفاده
از تنبرست در ABR برای تشخیص تغییرات زودهنگام مسمومیت
گوشی در الویت است.
Hatzopoulos
و همکاران (2002)
با بهکارگیری ABR و OAEبه بررسی تأثیر
سیسپلاتین بر شنوایی در نوعی رت پرداختند. در آن
تحقیق از تنپیپ در فرکانسهای 8000، 10000، 12000، 16000، 20000
و 30000
هرتز
استفاده شد و تعداد 20 رت مورد ارزيابي قرار گرفت که 16 رت تحت درمان با سیسپلاتین
بوده و چهار رت بهعنوان گروه شاهد در نظر گرفته شدند. نتایج حاکی از
تغییرات بارز در شاخصهایABR و OAE در 72 ساعت پس از دریافت دارو بود(14). در پژوهش حاضر،
مراجعۀ بیماران برای ارزیابی شنوایی،
حداکثر 72 ساعت پس از خاتمۀ دورۀ درمان با سیسپلاتین
یا کربوپلاتین بود و نتایج بهدست آمده، با یافتههای
تحقیق صورت گرفته توسط Hatzopoulos و همکاران (2002) مطابقت داشت. مشاهدۀ تغييرات بارز در
شنوايي در فاصله زماني 72 ساعت، حاكي از اثر زودهنگام اين خانواده دارويي، حتي پس
از يك يا دو سيكل از دريافت دارو، بر شنوايي بود كه يافتههاي ساير محققان نيز مؤید
آن است.
Knight و همکاران (2005) در تحقیقی به بررسی اثرات مسمومیت
گوشی (اتوتوکسیسیتی) مشتقات پلاتینیوم
پرداختند. در این تحقیق که روی 67 بیمار در محدودۀ
سنی هشت ماه تا 23 سال صورت گرفت، ادیومتری دورهای
متناسب با سن بیماران انجام شد. نتایج حاکی از کاهش شنوایی
دوطرفه در 61 درصد از بیماران بود(12). نظر به محدوديت سني و حال عمومي
بيماران شركتكننده در اين پژوهش، انجام ABR در اولويت
قرار داشت. در پژوهش حاضر، تمامی بیماران افت
شنوایی دوطرفه را حداقل در یک نوع محرک نشان دادند که مطابق با
الگوی مسمومیت گوشی اکثر داروها بود.
در
پژوهش حاضر تغییرات آستانه در رابطه با تفاوت بین گوش راست و چپ
معنیدار نبود. Schmidts و همکاران (2008) در تحقیقی به بررسی تفاوت دو گوشی
در تأثیرات سیسپلاتین بر شنوایی پرداختند. در
این تحقیق، از ادیومتری تن خالص، TEOAE
و DPOAE قبل و بعد از شیمیدرمانی استفاده شد. از 55
کودک شرکتکننده در این تحقیق (43 مرد و 21 زن) میانگین
آستانۀ شنوایی در تمامی 55 کودک در فرکانسهای 2000
تا 8000 هرتز در گوش چپ اندکی بالاتر بود. این تفاوت بین گوش
راست و چپ در فرکانسهای 4000، 6000 و 8000 هرتز بارز بود(15). نتایج
حاصل از پژوهش حاضر با تحقیقSchmidts و همکاران (2008) تطابق نداشت که میتواند بهدلیل
تعداد کم نمونه باشد.
نتیجهگیری
مشاهدۀ
تغييرات زودهنگام در آستانۀ شنوايي بيماران، بهويژه در فركانسهاي بالا،
نشاندهندۀ اثر نامطلوب داروهای شیمیدرمانی
خانوادۀ سیسپلاتین بر شنوایی و اهمیت پايش
شنوايي افراد تحت درمان با اين گروه دارويي با آزمونهایی با ويژگي
فركانسي است. نتایج این پژوهش در رابطه با تفاوت بین دو گوش، با
توجه به تعداد کم نمونهها، قابل تعمیم نیست.
سپاسگزاری
این
مقاله نتیجۀ طرح تحقیقاتی مصوب دانشگاه علوم پزشکی
تهران به شماره 1669806 مورخ 29/2/1389 است. دستاندرکاران این پژوهش مراتب
سپاس خود را نسبت به پرسنل محترم بیمارستان فوق تخصصی کودکان حضرت
علیاصغر (ع) بهویژه جناب آقای دکتر سلیمی و سرکار
خانم صانعی سرپرستار بخش خون و نیز والدین و کودکان بیمار
شرکتکننده در این تحقیق اعلام مینمایند.
1.
Rossof
AH, Slayton RE, Perlia CP. Preliminary clinical experience with
cis-diamminedichloroplatinum (II) (NSC 119875, CACP). Cancer.
1972;30(6):1451-6.
2.
Schaefer
SD, Post JD, Close LG, Wright CG. Ototoxicity of low- and moderate-dose
cisplatin. Cancer. 1985;56(8):1934-9.
3.
Rybak
LP, Whitworth CA,
Mukherjea D, Ramkumar V.
Mechanisms of cisplatin-induced ototoxicity and
prevention. Hear
Res. 2007;226(1-2):157-67.
4.
Truong
MT, Winzelberg J, Chang KW. Recovery
from cisplatin-induced ototoxicity: a case report and review. Int J Pediatr
Otorhinolaryngol. 2007;71(10):1631-8.
5.
Toral-Martiñón
R, Shkurovich-Bialik P, Collado-Corona MA, Mora-Magaña I, Goldgrub-Listopad
S, Shkurovich-Zaslavsky M. Distortion product otoacoustic emissions test is
useful in children undergoing cisplatin treatment. Arch Med Res. 2003;34(3):205-8.
6.
Fausti
SA, Reavis KM, Helt WJ, Gordon JS, Philips DS, Konrad-Martin DL. Audiologic monitoring for ototoxicity
and patient management. In: Campbell KCM, editor. Pharmacology
and ototoxicity for audiologists. 1st ed. New York: Thomson-Delmar
Learning; 2007. p. 231.
7.
Stavroulaki
P, Apostolopoulos N, Segas J, Tsakanikos M, Adamopoulos G. Evoked otoacoustic
emissions--an approach for monitoring cisplatin induced
ototoxicity in children. Int J Pediatr Otorhinolaryngol. 2001;59(1):47-57.
8.
Hall
J. New Handbook of auditory evoked responses. 1st ed. Boston: Allyn
& Bacon Education; 2007.
9.
Roeser
RJ, Valente M, Hosford DH. Audiology diagnosis. 2nd ed. New York:
Thieme Medical Publishers; 2007.
10.
Stelmachowicz
PG, Pittman AL, Hoover BM, Lewis DE, Moeller MP. The
importance of high-frequency audibility in the speech and language development
of children with hearing loss. Arch Otolaryngol Head Neck Surg.
2004;130(5):556-62.
11.
Kampbell
KCM. Audiologic monitoring for Ototoxicity. In: Roland PS, Rutka JA, editors. Ototoxicity. 1st ed. Hamilton: BC Decker Inc; 2004. p. 153-60.
12.
Knight
KR, Kraemer DF, Neuwelt EA. Ototoxicity in children receiving platinum
chemotherapy: underestimating a commonly occurring toxicity that may influence academic
and social development. J Clin Oncol. 2005;23(34):8588-96.
13.
Katzung
BG. Basic and clinical pharmacology. 8th ed. New York: McGraw-Hill;
2001.
14.
Hatzopoulos
S, Petruccelli J, Laurell G, Avan P, Finesso M, Martini A. Ototoxic effects of
cisplatin in a Sprague-Dawley rat animal model as revealed by ABR and
transiently evoked otoacoustic emission measurements.
Hear Res. 2002;170(1-2):70-82.
15.
Schmidt
CM, Knief A, Lagosch AK, Deuster D, am Zehnhoff-Dinnesen A. Left-right
asymmetry in hearing loss following cisplatin therapy in children--the left ear
is slightly but significantly more affected. Ear Hear. 2008;29(6):830-7.
 میانگین
آستانههای موج V برای محرک تنبرست 4000 هرتز قبل از دریافت دارو، در
گوش راست 50/40 با انحراف معیار 56/9 دسیبل SPL بود که پس از دریافت دارو، به 50/60 با انحراف معیار 99/14
دسیبل SPL رسید. مقادیر مذکور برای گوش
چپ، بهترتیب 50/46 و 50/65 با انحراف معیار 47/7 و 17/15 دسیبل
SPL بود. میانگین آستانههای موج Vبرای محرک تنبرست 8000
هرتز قبل از دریافت دارو، در گوش راست 50/56 با انحراف معیار 15/14
دسیبل SPL و پس از دریافت دارو 50/70 با انحراف معیار 791/12 دسیبل SPL بود. مقادیر مذکور برای گوش چپ بهترتیب 50/57 و
50/78 با انحراف معیار 75/12 و 33/17 دسیبل SPL بود. میانگین تغییرات آستانۀ موجV برای محرکهای کلیک، تنبرست 4000 هرتز و 8000 هرتز، بهترتیب
75/11 دسیبل SPL با انحراف معیار
635/9، 5/19 دسیبل SPL با انحراف معیار 659/13 و 5/17
دسیبل SPL با انحراف معیار 722/12 بهدست آمد. تغییرات
آستانه، قبل و بعد از دریافت دارو برای هر سه محرک کلیک و محرک
تنبرست 4000 و 8000 هرتز معنیدار بود(001/0p<) که در جدول 1 نشان داده شده است.
میانگین
آستانههای موج V برای محرک تنبرست 4000 هرتز قبل از دریافت دارو، در
گوش راست 50/40 با انحراف معیار 56/9 دسیبل SPL بود که پس از دریافت دارو، به 50/60 با انحراف معیار 99/14
دسیبل SPL رسید. مقادیر مذکور برای گوش
چپ، بهترتیب 50/46 و 50/65 با انحراف معیار 47/7 و 17/15 دسیبل
SPL بود. میانگین آستانههای موج Vبرای محرک تنبرست 8000
هرتز قبل از دریافت دارو، در گوش راست 50/56 با انحراف معیار 15/14
دسیبل SPL و پس از دریافت دارو 50/70 با انحراف معیار 791/12 دسیبل SPL بود. مقادیر مذکور برای گوش چپ بهترتیب 50/57 و
50/78 با انحراف معیار 75/12 و 33/17 دسیبل SPL بود. میانگین تغییرات آستانۀ موجV برای محرکهای کلیک، تنبرست 4000 هرتز و 8000 هرتز، بهترتیب
75/11 دسیبل SPL با انحراف معیار
635/9، 5/19 دسیبل SPL با انحراف معیار 659/13 و 5/17
دسیبل SPL با انحراف معیار 722/12 بهدست آمد. تغییرات
آستانه، قبل و بعد از دریافت دارو برای هر سه محرک کلیک و محرک
تنبرست 4000 و 8000 هرتز معنیدار بود(001/0p<) که در جدول 1 نشان داده شده است.